Trộn 150 ml dung dịch hỗn hợp NaOH 0,2M và KOH 0,2M với 250ml dung dịch HCl 0,4 M thu được dung dịch (X)
a/ Tính nồng độ các ion trong dung dịch (X)
b/ Tính pH của dung dịch (X)Trộn 100 ml dung dịch hỗn hợp HCl 0,2M và H2SO4 0,2M với 300 ml dung dịch NaOH 0,4 M thu được dung dịch (X)
a/ Tính nồng độ các ion trong dung dịch (X)
b/ Tính pH của dung dịch (X)a, \(n_{HCl}=0,1.0,2=0,02\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(n_{H_2SO_4}=0,1.0,2=0,02\left(mol\right)=n_{SO_4^{2-}}\) \(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,04\left(mol\right)\)
\(n_{NaOH}=0,3.0,4=0,12\left(mol\right)=n_{Na^+}=n_{OH^-}\)
\(\Rightarrow\sum n_{H^+}=0,02+0,04=0,06\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,06__0,06 (mol)
⇒ nOH- dư = 0,12 - 0,06 = 0,06 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\left[Cl^-\right]=\dfrac{0,02}{0,1+0,3}=0,05\left(M\right)\\\left[SO_4^{2-}\right]=\dfrac{0,02}{0,1+0,3}=0,05\left(M\right)\\\left[Na^+\right]=\dfrac{0,12}{0,1+0,3}=0,3\left(M\right)\\\left[OH^-\right]=\dfrac{0,06}{0,1+0,3}=0,15\left(M\right)\end{matrix}\right.\)
b, pH = 14 - (-log[OH-]) ≃ 13,176
Hỗn hợp dung dịch X gồm NaOH 0.1M và KOH 0.1M. Trộn 100 ml dung dịch X với 100 ml dung dịch
H2SO4 0.2M thu được dung dịch A.
a. Tính nồng độ các ion trong dung dịch A.
b. Tính pH của dung dịch A.
Hỗn hợp dung dịch X gồm NaOH 0.1M và KOH 0.1M. Trộn 100 ml dung dịch X với 100 ml dung dịch
H2SO4 0.2M thu được dung dịch A.
a. Tính nồng độ các ion trong dung dịch A.
b. Tính pH của dung dịch A.
a, \(\left[Na^+\right]=0,1\)
\(\left[K^+\right]=0,1\)
\(\left[OH^-\right]=0,2\)
\(\left[SO_4^{2-}\right]=0,2\)
\(\left[H^+\right]=0,4\)
b, \(n_{H^+}=0,1.0,4=0,04\left(mol\right)\)
\(n_{OH^-}=0,1.0,2=0,02\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(\Rightarrow n_{H^+dư}=0,02\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,02}{200}=10^{-4}\)
\(\Rightarrow pH=4\)
Hỗn hợp dung dịch X gồm NaOH 0.1M và KOH 0.1M. Trộn 100 ml dung dịch X với 100 ml dung dịch
H2SO4 0.2M thu được dung dịch A.
a. Tính nồng độ các ion trong dung dịch A.
b. Tính pH của dung dịch A.
$n_{NaOH} = n_{KOH} = 0,1.0,1 = 0,01(mol)$
$n_{H_2SO_4} = 0,02(mol)$
OH- + H+ → H2O
Bđ : 0,01...0,04..................(mol)
Pư : 0,01...0,01...................(mol)
Sau pư : 0......0,03...................(mol)
$V_{dd} = 0,1 + 0,1 = 0,2(lít)$
Vậy :
$[K^+] = [Na^+] = \dfrac{0,01}{0,2} = 0,05M$
$[H^+] = \dfrac{0,03}{0,2} = 0,15M$
$[SO_4^{2-}] = \dfrac{0,02}{0,2} = 0,1M$
b)
$pH = -log(0,15) = 0,824$
Câu 32: Trộn 250ml dung dịch A gồm Ba(OH)2 0,2M và NaOH 0,3M với 250ml dung dịch H_{2}*S*O_{4} có pH = 1 Sau khi trộn thu được dung dịch B và m (g) kết tủa. a) Tính pH của dung dịch A. b) Tính nồng độ các ion trong dung dịch thu được. c) Tính pH của dung dịch thu được d) Tính m Giúp em với ạ
Trộn 200 ml dung dịch NaOH 0,1M với 300 ml dung dịch HCl 0,2M thu được dung dịch A.
a. Tính nồng độ các ion trong dung dịch A.
b. Tính pH của dung dịch A.
nH+=0,06 mol nOH-=0,02 mol
H+ + OH- ---> H2O
0,06 0,02
0,02 0,02 0,02
0,04
[H+] du=0,04/0,5=0,08 M
[Na+]=0,02/0,5=0,04M
[Cl-]=0,06/0,5=0,12M
pH= -log(0,08)=1,09
Trộn ba dung dịch: HCl 0,2M; H 2 SO 4 0,1M và HNO 3 0,08M với thể tích bằng nhau thu được dung dịch X. Cho 150 ml X tác dụng với 150 ml dung dịch hỗn hợp NaOH 0,1M và KOH 0,058M thu được dung dịch Y có pH = x. Giá trị của x là
A. 4
B. 1
C. 2
D. 3
Chọn D
Trộn 3 dung dịch với thể tích bằng nhau thu được 150 ml dung dịch X → mỗi dung dịch lấy 50ml.
→ n H + = 0,05.0,2 + 0,05.2.0,1 + 0,05.0,08 = 0,024 mol.
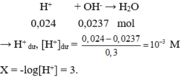
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4, 0,05M và HCL 0,1M với 100 ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M, được dung dịch X. Tính giá trị pH của dung dịch X và tính khối lượng kết tủa thu được.
`100mL=0,1L`
`n_{H^+}=0,1.0,05.2+0,1.0,1=0,02(mol)`
`n_{SO_4^{2-}}=0,1.0,05=0,005(mol)`
`n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04(mol)`
`n_{Ba^{2+}}=0,1.0,1=0,01(mol)`
`Ba^{2+}+SO_4^{2-}->BaSO_4`
Do `0,01>0,005->` Tính theo `SO_4^{2-}`
`n_{BaSO_4}=n_{SO_4^{2-}}=0,005(mol)`
`->m_↓=0,005.233=1,165(g)`
`H^{+}+OH^{-}->H_2O`
Do `0,02<0,04->OH^-` dư
`n_{OH^{-}\ pu}=n_{H^+}=0,02(mol)`
`->n_{OH^{-}\ du}=0,04-0,02=0,02(mol)`
Trong X: `[OH^-]={0,02}/{0,1+0,1}=0,1M`
`->pH=14-pOH=14+lg[OH^-]=13`
Bài 2: Trộn lẫn 300ml dung dịch HCl 0,2M với 200ml dung dịch H2SO4 0,05M thu được dung dịch X. Tính pH của dung dịch X.
Bài 3:Trộn lẫn 150 ml dung dịch NaOH 2M với 200 ml dung dịch H2SO4 1M, thu được dung dịch X. Tính giá trị pH dung dịch X.
Bài 4: Cho 200 ml dung dịch NaHCO3 1M tác dụng với dung dịch Ba(OH)2 dư thu được m gam kết tủa trắng. Tìm giá trị của m.
Bài 5: Hòa tan hết 9,9 gam Zn(OH)2 cần vừa đủ V ml dung dịch HCl 2M. Tìm giá trị của V.